식품의약품안전처(처장 정승)는 2013년 제네릭의약품 개발을 위한 ‘생물학적 동등성시험’ 계획 승인 현황을 분석한 결과, 승인건수는 총 163건으로 2012년 201건에 비해 19%정도 감소했다고 7일 밝혔다.
이에 대해 식약처는 2013년의 재심사 만료 오리지널 의약품수가 감소했고, 여러 회사가 공동으로 생동성시험을 진행함에 따른 것이라고 분석했다.
또한, 식약처는 지난해 제네릭의약품의 개발경향에 대해 ▲특허 및 재심사 만료의약품 ▲고혈압, 고지혈증 등 심혈관계의약품 ▲치매 및 우울장애치료제 ▲위ㆍ십이지장궤양치료제 등에 집중됐다고 설명했다.
식약처의 분석자료에 따르면 성분별 승인건수는 오는 4월 특허 만료예정인 고지혈증치료제의 주성분 ‘로수바스타틴칼슘’이 12건(7.4%)으로 가장 많았고, 8월에 재심사가 만료되는 고혈압치료제의 주성분인 ‘암로디핀베실산염ㆍ올메사르탄메독소밀’가 10건(6.1%)으로 뒤를 이었다.
이외에 소화성궤양치료제인 ‘구연산비스마스칼륨라니티딘염산염ㆍ수크랄페이트’와 치매치료제인 ‘리바스티그민’이 각각 7건(4.3%)으로 나왔다.
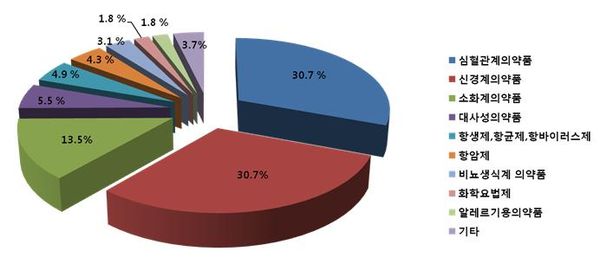
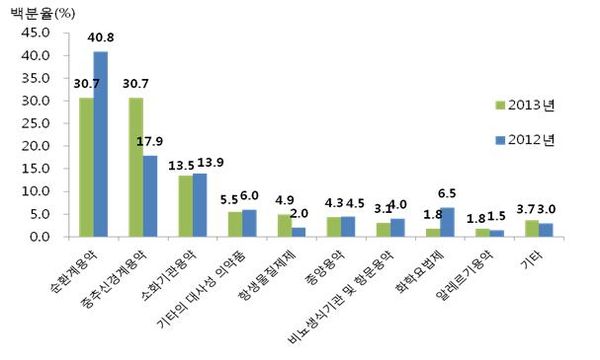
치료영역별 승인건수는 심혈관계의약품 50건(30.7%), 정신신경계의약품 50건(30.7%), 소화계의약품 22건(13.5%) 등의 순서로 많았다. 이중 고지혈증 및 고혈압치료제 등 심혈관계의약품은 2012년(82건)에 비해 39% 줄어들었다.
치매, 불안 및 우울장애, 간질치료제 등 정신신경계의약품의 경우, 고령화 사회 및 현대 사회 스트레스 증가에 따라 50건(30.7%)이 승인됐으며, 2012년(39건)에 비해 28% 증가했다.
위ㆍ십이지장궤양 치료제 등 소화계의약품은 스트레스 및 불규칙한 식습관 등으로 인한 소화기계 질환의 증가로 22건(13.5%) 승인됐으며, 2012년(28건)에 비해 21% 감소했다.
아울러 지난해 생동성시험 승인을 처음으로 받은 성분은 항생제 ‘리팍시민’ (4건), 관절염치료제 ‘나프록센/에스오메프라졸마그네슘’(1건), 발기부전치료제 ‘타다라필’ (2건) 등 7건이었다.
복합제의 경우, 총 34건이 승인됐으며, 심혈관계의약품이 22건(64.7%)으로 가장 많았다.
식약처는 “향후에도 고혈압, 치매 등 고령화 사회에서 발병률이 증가하는 만성질환 치료제와 스트레스 증가 등에 따른 우울장애치료제 및 위ㆍ십이지장궤양치료제 개발에 집중이 계속될 것으로 보인다.”라고 설명했다.

